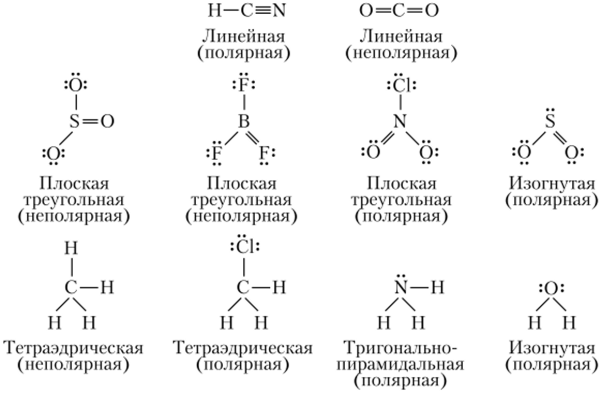
Для изучения трехмерных свойств аминокислотных последовательностей, содержащихся в белках и маломолекулярных органических соединениях, применяют высокоразрешающее исследование молекул с помощью атомного магнитного поля. Этот подход позволяет извлекать подробную информацию о пространственном расположении атомов, а также их взаимодействиях внутри молекулы, что способствует точному прогнозированию их функций. Таким образом, такой метод является незаменимым инструментом для анализа сложных молекул в области биохимии и молекулярной биологии.
Важнейшей характеристикой этого метода является его способность выявлять специфические особенности взаимодействий, которые нельзя определить другими методами. Применяя соответствующие технологии, можно с высокой степенью уверенности определить местоположение различных групп атомов в молекуле, что предоставляет точные данные для построения карт молекулярных сетей и понимания механизмов биохимических процессов.
Использование современных подходов в исследовании структурных аспектов молекул открывает широкие возможности для создания более эффективных лекарственных препаратов и молекул с заданными свойствами. Применяя этот метод, можно не только улучшить качество диагностики и терапии, но и ускорить разработку новых биологически активных веществ, значительно повысив точность их синтеза и предсказуемость биологического действия.
Облако тегов
Применение ЯМР для изучения вторичной конформации молекул
Подготовка образцов и условия эксперимента
Для успешного применения метода необходимо обеспечить оптимальные условия для образцов, такие как растворение в подходящих буферах и поддержание стабильности молекул в ходе измерений. Кроме того, важным аспектом является использование определённых изотопов, таких как 13C и 15N, которые позволяют отслеживать взаимодействия в аминокислотных остатках и уточнять пространственное расположение отдельных структурных элементов.
Спектральная обработка и интерпретация данных
Основные характеристики, которые помогают в определении конформации, включают химические сдвиги, разделение сигналов по времени и зависимость их изменения от конформационных переходов. Анализ многомерных спектров позволяет более точно выявить локальные взаимодействия, что особенно важно при анализе гибких или частично упорядоченных молекул. При этом учитываются данные с различных типов спектров: одно- и многомерных (2D, 3D).
Для точного расчёта вторичных элементов структуры используется сводная информация о спектрах, включая сигналы от водородных и углеродных атомов, что даёт возможность точно определить конформацию. Использование специализированных программных пакетов значительно облегчает анализ полученных данных и ускоряет интерпретацию результатов.
Практическое применение метода в биологии
Технология находит широкое применение в биохимии и фармакологии для исследования взаимодействий молекул с лигандами, а также для детектирования изменений в молекулярной конформации при связывании с другими молекулами. Полученные данные часто используются для разработки новых терапевтических средств, основанных на знании молекулярной структуры и взаимодействий с белками.
Облако тегов
| Конформация | Молекулы | Изотопы | Сигналы | Анализ |
| Спектры | Взаимодействия | Гибкость | Программное обеспечение | Фармакология |
| Белки | Лиганды | Гибкость молекул | Спектроскопия | Решение |
Методы улучшения разрешающей способности при анализе пептидов
Для повышения качества спектров и увеличения разрешающей способности при исследовании пептидов рекомендуется использовать методы, направленные на улучшение чувствительности сигналов и снижение фона. В первую очередь стоит обратить внимание на применение многократных измерений с повышением длительности эксперимента, что позволяет улучшить точность результатов и уменьшить шум. Кроме того, применение высококачественных магнитных полей с минимальными флуктуациями также способствует увеличению разделения пиков в спектре.
Одним из эффективных методов является использование различных типов пулов (измерений) с адаптивной настройкой параметров для конкретного образца. В частности, адаптация спектроскопии с высокой частотой возбуждения помогает уменьшить перекрытия сигналов, что важно при изучении сложных молекул. Также стоит учитывать важность точной настройки температуры, так как колебания могут сильно влиять на спектральные особенности молекул.
Использование специальных методов обработки данных, таких как 2D или 3D спектроскопия, позволяет значительно улучшить разрешение в исследуемых образцах. Эти методики помогают более детально разделить пики, что особенно важно при анализе многокомпонентных смесей. Дополнительное улучшение разрешающей способности также возможно при использовании различных вариантов экспериментальных подходов, таких как корреляционные и сдвиговые методы, которые эффективно уменьшают ширину линий и повышают контраст.
Для увеличения разрешающей способности также стоит применять методы изотопного помечания, что позволяет выделить отдельные элементы молекулы и повысить их интенсивность в спектре. Это дает возможность отделить пики, которые могли бы сливаться из-за схожести химических сдвигов.
Облако тегов
Роль изотопных маркеров в ЯМР-исследованиях структуры пептидов
Для улучшения качества спектров и повышения точности анализа соединений с использованием ЯМР, изотопные маркеры служат важным инструментом. Введение стабильных изотопов в молекулы позволяет детализировать информацию о конформации и динамике, а также получить точные данные о взаимодействиях атомов. Применение изотопов углерода (13C) и азота (15N) особенно эффективно для решения сложных задач в области молекулярной биологии.
Основным преимуществом таких меток является возможность избирательного отслеживания конкретных атомов или фрагментов молекулы. Это позволяет избежать перекрытия сигналов и помогает получить более четкие спектры. Например, замена водорода на тяжелый водород (2H) позволяет избежать перекрестных взаимодействий между атомами водорода, что значительно улучшает разрешение спектра.
Метки 13C и 15N дают возможность точно определять расстояния между атомами, используя ядерное спин-спин взаимодействие, что существенно повышает качество 2D и 3D спектров. Это позволяет исследователям более точно реконструировать пространственную организацию молекул, что важно для понимания их биологических функций.
Кроме того, использование изотопных маркеров помогает проводить мульти-изотопное меткирование, которое позволяет комбинировать данные различных типов ЯМР-спектров, таких как 1H-13C и 1H-15N, для более детализированного анализа. Это особенно важно для изучения больших и сложных молекул, где стандартные методы могут быть неэффективными.
Важно учитывать, что применение изотопных маркеров требует определенных затрат, так как синтез таких молекул часто сложен и дорог, однако для получения высококачественных данных они являются незаменимым инструментом. Молекулы с метками стабильных изотопов также могут быть использованы для изучения динамики молекул в реальных условиях, что дает возможность понять механизмы их взаимодействий в живых системах.